Abstrak
Kit uji cepat Dengue Duo komersial dievaluasi untuk diagnosis dini dengue dengan mendeteksi antigen NS1 virus dengue dan antibodi imunoglobulin M (IgM)/IgG. Sebanyak 420 sampel serum pasien menjalani uji reaksi berantai polimerase transkripsi balik waktu nyata (RT-PCR), uji imunosorben terkait enzim penangkap IgM (ELISA) internal, uji penghambatan hemaglutinasi, dan uji cepat SD Dengue Duo. Dari 320 serum dengue akut dan konvalesen, infeksi dengue terdeteksi baik melalui serologi maupun RT-PCR pada 300 sampel (93,75%), dibandingkan dengan 289 sampel (90,31%) pada kombinasi SD Duo NS1/IgM. Laju deteksi NS1 berbanding terbalik, sedangkan laju deteksi IgM berbanding lurus dengan keberadaan antibodi IgG. Sensitivitas dan spesifisitas dalam mendiagnosis infeksi dengue akut dengan SD Duo NS1/IgM masing-masing adalah 88,65% dan 98,75%. Uji ini sensitif dan sangat spesifik. Deteksi NS1 dan IgM oleh SD Duo memberikan tingkat deteksi yang sebanding baik melalui serologi maupun RT-PCR.
Perkenalan
Prevalensi dengue global telah tumbuh secara dramatis dalam beberapa dekade terakhir. Penyakit ini sekarang endemik di lebih dari 100 negara di Afrika, Amerika, Mediterania Timur, Pasifik Barat, dan khususnya di Asia Tenggara. Organisasi Kesehatan Dunia (WHO) memperkirakan bahwa lebih dari 2,5 miliar orang berisiko terkena infeksi dengue dengan 50–100 juta kasus terjadi setiap tahunnya. Di antara infeksi ini, sekitar 250.000–500.000 kasus adalah demam berdarah dengue (DBD), dengan 24.000 kematian yang sebagian besar terjadi pada anak-anak. 1 , 2 Salah satu alasan terpenting untuk peningkatan kasus kemungkinan besar disebabkan oleh pembangunan dan urbanisasi yang cepat, yang menyediakan tempat berkembang biak bagi Aedes aegypti , vektor nyamuk utama yang bertanggung jawab atas penularan virus dengue (DENV). Penyebaran infeksi juga diperparah oleh perjalanan udara modern dan perdagangan internasional seperti ban kendaraan bermotor, yang memudahkan penularan individu yang terinfeksi dan larva nyamuk ke daerah yang tidak terinfeksi, sehingga menimbulkan risiko masuknya virus dan vektornya.
Oleh karena itu, pola yang muncul dan tren peningkatan insiden infeksi dengue ini sangat memprihatinkan karena belum ada pengobatan spesifik untuk dengue, dan sebagian besar terapi bersifat suportif. Lebih lanjut, vaksin berlisensi belum tersedia.
Terdapat empat serotipe dengue (DENV-1, DENV-2, DENV-3, DENV-4) yang dapat menyebabkan penyakit pada manusia, mulai dari yang sembuh sendiri hingga demam berdarah dengue dan sindrom syok dengue (DHF/DSS) yang mengancam jiwa. Demam dengue (DD) klasik umumnya sembuh sendiri dan ditandai dengan demam serta berbagai tanda dan gejala nonspesifik seperti sakit kepala, malaise, lemas, ruam, dan nyeri badan. DHF dibedakan dari DD dengan timbulnya kebocoran plasma, trombositopenia yang nyata, dan diatesis perdarahan. Kebocoran plasma yang parah dapat menyebabkan syok, dengan angka kematian pada pasien yang tidak diobati bervariasi antara 10% dan 20%, tetapi dapat mencapai 40% jika disertai syok. Namun, angka tersebut dapat diminimalkan menjadi 0,2% di rumah sakit dengan staf yang terlatih dalam menangani penyakit ini .
Dengan meningkatnya insiden infeksi dengue, konfirmasi diagnostik dini infeksi dengue pada pasien memungkinkan intervensi klinis yang tepat waktu, investigasi etiologi, dan pengendalian penyakit. Oleh karena itu, diagnosis penyakit dengue selama fase akut harus menjadi prioritas dan merupakan masalah kesehatan masyarakat. Beberapa pendekatan telah diterapkan untuk diagnosis laboratorium infeksi virus dengue. Metode-metode ini meliputi deteksi virus (dengan kultur sel, imunofluoresensi), deteksi antigen virus (dengan uji imunosorben terkait enzim [ELISA]), deteksi antibodi anti-virus dengue (dengan penghambatan hemaglutinasi [HI], uji fiksasi komplemen [CF], uji netralisasi, ELISA), dan deteksi asam nukleat virus (dengan reaksi berantai polimerase transkripsi balik waktu nyata [RT-PCR]). Namun, untuk diagnosis dengue yang dikonfirmasi, DENV harus diidentifikasi dengan isolasi atau deteksi asam nukleat atau harus ada peningkatan 4 kali lipat titer antibodi dengan serum berpasangan pada pasien yang menunjukkan tanda dan gejala yang konsisten dengan infeksi virus dengue. Baru-baru ini, kit yang tersedia secara komersial telah dikembangkan untuk deteksi cepat infeksi dengue.4 – 8 Kit ini dirancang berdasarkan prinsip mendeteksi keberadaan antigen NS1 dan/atau antibodi anti-dengue dalam darah pasien yang diduga menderita dengue .
NS1 adalah glikoprotein yang sangat terkonservasi yang hadir pada konsentrasi tinggi dalam serum pasien yang terinfeksi dengue selama fase klinis awal penyakit, dan ditemukan dari Hari ke-1 hingga Hari ke-9 setelah timbulnya demam dalam sampel pasien yang terinfeksi dengue primer atau sekunder. 9 , 10 IgM menjadi terdeteksi pada Hari ke-3 hingga ke-5 penyakit dalam kasus infeksi dengue primer dan bertahan selama 2 hingga 3 bulan, sedangkan IgG muncul pada hari keempat belas dan bertahan seumur hidup. Infeksi sekunder menunjukkan bahwa IgG meningkat dalam 1 hingga 2 hari setelah timbulnya gejala, bersamaan dengan antibodi IgM. Oleh karena itu, pasien dengan infeksi sekunder akan memiliki hasil IgG positif, biasanya, tetapi tidak selalu dengan hasil IgM positif. 11 – 13
Dalam studi ini, kit diagnostik dengue cepat yang tersedia secara komersial, perangkat kombo SD BIOLINE Dengue Duo (Standard Diagnostic Inc., Korea), yang dirancang untuk mendeteksi antigen NS1 dengue dan antibodi IgM/IgG, dievaluasi potensi aplikasinya untuk diagnosis dini infeksi virus dengue akut berdasarkan sampel serum akut tunggal. Evaluasi dilakukan dengan mengacu pada metode uji diagnostik laboratorium yang ada, seperti isolasi virus dengue, RT-PCR waktu nyata, ELISA penangkapan IgM internal (MAC-ELISA), dan HI.
Bahan dan Metode
Spesimen serum.
Sebanyak 420 serum digunakan dalam evaluasi ini. Sampel darah ini dikumpulkan dari pasien yang dirawat di University Malaya Medical Center (UMMC), Kuala Lumpur, Malaysia, karena infeksi virus akut. Serum ini terdiri atas 1) 30 sampel yang darinya virus dengue diisolasi, 2) 50 sampel positif untuk RNA virus dengue melalui RT-PCR, 3) 50 sampel yang darinya antigen dengue NS1 dideteksi positif oleh antigen Platelia Dengue NS1 (Bio-Rad Laboratories, Marnes-la-Coquette, Prancis) dan pan-E dengue early ELISA (Panbio, Queensland, Australia), 4) 50 sampel yang negatif IgM tetapi sero-konversi dalam serum konvalesen, 5) 10 pasang dengue primer yang terkonfirmasi, 6) 10 pasang dengue sekunder yang terkonfirmasi, 7) 100 sampel acak yang IgM-nya terdeteksi terhadap dengue, 8) 20 sampel yang didiagnosis secara klinis sebagai dengue tetapi diuji laboratorium sebagai negatif, dan 9) 80 sampel dari donor sehat dan pasien dengan infeksi selain dengue ( Tabel 1A dan B ). Semua sampel menjalani isolasi virus, MAC-ELISA internal, RT-PCR dengue real-time internal, dan uji HI. Persetujuan tertulis diperoleh dari pasien. Persetujuan etik diberikan oleh Komite Ilmiah dan Etika di UMMC, dengan prosedur yang dilaksanakan sesuai dengan Deklarasi Helsinki tahun 1975, sebagaimana direvisi pada tahun 2000.14
Tabel 1A.
Sampel serum yang digunakan untuk evaluasi kit SD BIOLINE Dengue Duo
| Kategori | Nomor sampel (n) |
|---|---|
| (a) Serum akut dari mana virus dengue diisolasi | 30 |
| (b) Serum PCR positif Dengue | 50 |
| (c) Serum positif antigen Dengue NS1 | 50 |
| (d) Sampel akut sero-negatif (IgM negatif), tetapi sampel konvalesen sero-konversi | 50 |
| (e) Serum demam berdarah primer (10 pasang) | 20 |
| (f) Serum dengue sekunder (10 pasang) | 20 |
| (g) Serum IgM positif (rasio P/N bervariasi) * | 100 |
| (h) Secara klinis demam berdarah tetapi hasil laboratorium negatif | 20 |
| (i) Agen penyakit lain dan donor sehat (kontrol negatif) | 80 |
| Total | 420 |
Rasio P/N (rasio positif:negatif): Rasio AP/N yang lebih besar dari atau sama dengan 2,0 dianggap positif; hasil dengan rasio P/N kurang dari 2 dilaporkan sebagai negatif.
Tabel 1B.
Panel kontrol negatif *
| Agen penyakit lain dan donor sehat | Nomor sampel (n) |
|---|---|
| (a) Virus BK | 10 |
| (b) Virus sitomegalo (CMV) | 10 |
| (c) Campak | 2 |
| (d) Virus Epstein-Barr | 10 |
| (f) Ensefalitis Jepang | 11 |
| (g) Chikungunya | 7 |
| (h) Virus herpes simpleks (HSV) | 3 |
| (i) Infeksi ganda CMV dan HSV | 1 |
| (j) Nipah IgG positif | 5 |
| (k) Leptospirosis | 1 |
| (l) Ricketsia | 1 |
| (m) S. typhi (n) West Nile | 36 |
| (o) Donor sehat | 10 |
| Total | 80 |
Tabel menunjukkan 15 kelompok kontrol negatif dan jumlah sampel serum yang digunakan untuk evaluasi dalam penelitian ini.
Isolasi virus.
Isolasi virus dilakukan dengan menginokulasikan 5 μL serum akut ke dalam galur sel nyamuk C6/36 yang konfluen dan diinkubasi pada suhu 28°C selama 7 hingga 10 hari. Antigen dengue kemudian dideteksi secara imunofluoresensi dengan antibodi monoklonal spesifik dengue yang diperoleh dari Pusat Pengendalian dan Pencegahan Penyakit (Foothills Campus, Fort Collins, CO). 15 , 16
Uji penghambatan hemaglutinasi internal.
Uji HI dilakukan seperti yang dijelaskan sebelumnya. 17 Singkatnya, 25 μL bovine albumin borate saline (BABS) 0,4% ditambahkan ke dalam sumur 2 hingga 12 dari pelat mikrotiter ELISA 96 sumur. Lima puluh mikroliter dan 25 μL serum yang diekstraksi dengan aseton ditambahkan masing-masing ke dalam sumur 1 dan 12, dan serum dititrasi dari sumur 1 hingga sumur 12. Dua puluh lima mikroliter antigen ditambahkan ke dalam 11 sumur pertama sementara BABS ditambahkan ke dalam sumur terakhir (kontrol serum), setelah itu pelat ditutup dan diinkubasi pada suhu 4°C selama 18 hingga 24 jam. Goose RBC yang baru disiapkan (50 μL) ditambahkan ke dalam semua sumur dan pelat mikrotiter diinkubasi lebih lanjut pada suhu 37°C selama 45 menit, sebelum menginterpretasikan hasilnya. Hasil diinterpretasikan sesuai dengan pedoman WHO. 18
ELISA penangkapan IgM internal (MAC-ELISA).
ELISA MAC in-house dilakukan seperti yang dijelaskan sebelumnya.19 Singkatnya , 100 μL sampel dengan pengenceran 1:100 ditambahkan ke dalam pelat dasar U 96-sumur berlapis anti-IgM manusia dan diinkubasi pada suhu 37°C selama 1 jam. Setelah dicuci tiga kali dengan PBS-Tween 20 (0,05%), 100 μL antigen dengue dengan pengenceran 1:100 ditambahkan dan kemudian diinkubasi pada suhu 37°C selama satu jam lagi. Pelat kemudian dicuci tiga kali dengan PBS-Tween 20 (0,05%), diikuti dengan penambahan 100 μL antibodi monoklonal tikus anti-dengue dengan pengenceran 1:5000 dan inkubasi lebih lanjut pada suhu 37°C selama 1 jam. Pelat dicuci kembali dengan PBS-Tween 20 (0,05%) dan ditambahkan 100 μL pengenceran 1:50.000 IgG anti-tikus kambing terkonjugasi dengan horseradish peroxidase (HRP), sebelum diinkubasi selama 1 jam pada suhu 37°C. Setelah tiga kali pencucian tambahan, 100 μL OPD (o-fenilendiamin 2HCl) ditambahkan ke semua sumur dan diinkubasi dalam gelap pada suhu ruang. Reaksi dihentikan dengan 50 μL asam sulfat 4N dan absorbansi (OD) setiap sumur dibaca pada λ490 nm dengan filter referensi 630 nm menggunakan pembaca ELISA. Rasio positif terhadap negatif kemudian dihitung. OD kontrol positif/sampel dibagi dengan rata-rata OD negatif untuk mendapatkan rasio positif:negatif (P/N). Rasio AP/N yang sama atau lebih besar dari 2,0 dianggap positif. Hasil dengan rasio P/N kurang dari 2,0 dilaporkan negatif jika sampel dikumpulkan dua minggu setelah timbulnya penyakit.
RT-PCR waktu nyata.
RT-PCR real-time SYBR green I satu langkah dilakukan dalam thermocycler iCycler (Bio-Rad Laboratories, Hercules, CA) menggunakan iScript one-step RT-PCR Kit dengan SYBR Green I (Bio-Rad Laboratories), seperti yang dijelaskan oleh Yong dan lainnya. 20 Secara singkat, 5 μL RNA sampel yang diekstraksi ditambahkan ke reaksi 25 μL yang mengandung 1 × SYBR Green I, 75 nM dari setiap primer, dan 3 mM MgCl 2 . Kondisi siklus termal terdiri dari transkripsi balik 30 menit pada 50 °C, 15 menit aktivasi polimerase Taq pada 95 °C, diikuti oleh 45 siklus PCR pada 95 °C denaturasi selama 30 detik, 60 °C annealing selama 30 detik, dan ekstensi 72 °C selama 1 menit. Setelah amplifikasi, kurva leleh dianalisis. Hal ini dilakukan untuk memverifikasi spesifisitas produk PCR dengan melihat Tm-nya. Analisis kurva leleh terdiri dari tahap denaturasi pada suhu 95°C selama 1 menit, diturunkan menjadi 55°C selama 30 detik, dan diikuti oleh 80 siklus inkubasi dengan peningkatan suhu hingga 95°C pada laju 0,5°C/10 detik/siklus. Tm setiap produk PCR spesifik dianalisis menggunakan perangkat lunak sistem optik iCycler iQ versi 3.0a (Bio-Rad Laboratories). Tm untuk setiap sampel digunakan untuk mengidentifikasi serotipe dengue, dan sampel yang memiliki Tm yang sama diinterpretasikan memiliki serotipe yang sama.
Tes SD BIOLINE Dengue Duo NS1 Ag dan IgG/IgM.
Kit uji cepat SD BIOLINE Dengue Duo diproduksi oleh Standard Diagnostics dan merupakan uji imunokromatografi satu langkah yang dirancang untuk mendeteksi antigen NS1 virus dengue dan antibodi IgM/IgG diferensial terhadap virus dengue dalam darah lengkap manusia, serum, atau plasma. Tes cepat SD BIOLINE Dengue Duo berisi dua perangkat uji; sisi kiri untuk uji antigen NS1 dengue, sedangkan sisi kanan untuk uji IgG/IgM dengue. Kit ini dirancang berdasarkan prinsip bahwa ketika spesimen ditambahkan ke sumur sampel, IgG dan IgM anti-dengue dalam spesimen akan bereaksi dengan protein selubung virus dengue rekombinan-konjugat emas koloid dan membentuk kompleks antibodi-antigen. Kompleks ini akan ditangkap oleh IgG anti-manusia dan/atau IgM anti-manusia yang relevan yang diimobilisasi pada perangkat uji dan menghasilkan garis berwarna ketika bermigrasi sepanjang perangkat uji dengan aksi kapiler. Demikian pula, antigen dengue NS1 yang ditangkap oleh konjugat emas koloid anti-dengue NS1 Ag akan bermigrasi sepanjang perangkat hingga ditangkap oleh antigen anti-dengue NS1 yang diimobilisasi pada strip membran dan menghasilkan garis warna. Semua pengujian dalam penelitian ini dilakukan sesuai dengan petunjuk produsen. Secara singkat, untuk perangkat SD BIOLINE dengue NS1 Ag, 100 μL sampel uji ditambahkan ke dalam sumur sampel (S). Hasil uji diinterpretasikan pada 15–20 menit. Demikian pula, untuk perangkat SD BIOLINE dengue IgG/IgM, 10 μL sampel uji ditambahkan ke dalam sumur sampel (S). Ini diikuti dengan penambahan 4 tetes (90–120 μL) pengencer uji ke dalam sumur pengencer uji berbentuk bulat. Hasil diinterpretasikan pada 15–20 menit. Hasil uji diperiksa dan diinterpretasikan sesuai dengan petunjuk produsen oleh tiga pembaca yang berbeda untuk menghindari bias.
Analisis data.
Tabulasi, pengelolaan, dan analisis data mentah dilakukan menggunakan Microsoft Excel (Microsoft Inc., Redmond, WA). Analisis statistik dilakukan dengan Statistica versi 18 (StatSoft, Inc., Tulsa, OK). Sensitivitas, spesifisitas, efisiensi, nilai prediksi positif (VPP), dan nilai prediksi negatif untuk uji tersebut dihitung berdasarkan “sampel dengue positif sejati” (isolasi virus/positif PCR, serum akut sero-negatif, primer akut, sekunder akut) menggunakan rumus berikut:
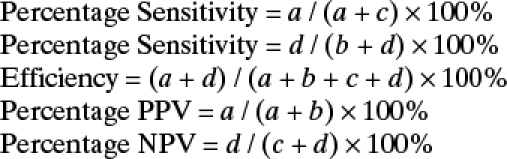 |
Di mana
 |
Hasil
Sebanyak 420 sampel yang dikumpulkan dari tahun 2007 hingga tahun 2009 dipilih untuk evaluasi kit uji cepat SD BIOLINE Dengue Duo. Evaluasi kit uji cepat SD dinilai terhadap panel sampel termasuk positif sejati dengan uji standar seperti isolasi virus dan RT-PCR waktu nyata, serum positif IgM, serum positif antigen NS1, dan serum yang berasal dari donor sehat dan agen penyakit lainnya. Hasilnya dirangkum dalam Tabel 2. Dari 320 serum untuk dengue, 168 (52,5%) dinyatakan positif untuk SD Duo NS1 Ag, dan 220 (68,75%) dinyatakan positif untuk SD Duo IgM. Strategi diagnostik yang menggabungkan SD Duo NS1 atau IgM (NS1/IgM) memberikan deteksi positif 289 (90,31%). Sebagai perbandingan, infeksi dengue terdeteksi dengan MAC-ELISA atau RT-PCR pada 300 sampel (93,75%), dengan MAC-ELISA pada 229 sampel (71,56%), dan dengan RT-PCR pada 162 sampel (50,63%). Di antara 30 sampel yang positif isolasi virus, SD Duo NS1/IgM mendeteksi 21 sampel (70%) positif. Satu sampel dari kategori yang secara klinis dengue tetapi hasil tes laboratorium negatif, dan sampel lain dari panel kontrol negatif juga dinyatakan positif oleh kit SD Dengue Duo.
Tabel 2.
Perbandingan kit SD BIOLINE Dengue Duo dengan MAC-ELISA dan RT-PCR internal *
| Kategori sampel | Angka (n) | Jumlah sampel yang dites positif, n (%) | |||||
|---|---|---|---|---|---|---|---|
| MAC-ELISA | RT-PCR | SD DUO NS1 | SD DUO IgM | SD DUO IgG | SD DUO NS1/IgM | ||
| Isolasi virus dengue positif | 30 | 9 (30) | 30 (100) | 18 (60) | 11 (36) | 9 (30) | 21 (70) |
| Dengue RT-PCR positif | 50 | 46 (92) | 50 (100) | 22 (44) | 40 (80) | 37 (74) | 44 (88) |
| Dengue NS1 positif † | 50 | 34 (68) | 35 (70) | 39 (78) | 33 (66) | 19 (38) | 47 (94) |
| Sampel akut sero-negatif tetapi sero-konversi konvalesen | 50 | 0 (0) | 37 (74) | 43 (86) | 7 (14) | 9 (18) | 46 (92) |
| Serum IgM positif dengue | 100 | 100 (100) | 1 (1) | 28 (28) | 92 (92) | 84 (84) | 93 (93) |
| Demam berdarah primer | 20 | 20 (100) | 6 (30) | 17 (85) | 19 (95) | 4 (20) | 20 (100) |
| Demam berdarah sekunder | 20 | 20 (100) | 3 (15) | 1 (5) | 18 (90) | 20 (100) | 18 (90) |
| Secara klinis demam berdarah tetapi hasil laboratorium negatif | 20 | 0 (0) | 0 (0) | 1 (5) | 0 (0) | 0 (0) | 1 (5) |
| Serum non-dengue (panel negatif) | 80 | 0 (0) | 0 (0) | 1 (1.7) | 0 (0) | 2 (3.4) | 1 (1.7) |
MAC-ELISA = uji imunosorben terkait-enzim penangkapan IgM internal; RT-PCR = reaksi berantai polimerase transkripsi terbalik.
Serum positif NS1 dikonfirmasi oleh antigen Platelia Dengue NS1 (Laboratorium Bio-Rad, Marnes-la-Coquette, Prancis) dan uji ELISA dini dengue pan-E (Panbio, Queensland, Australia).
Analisis kinerja SD Dengue Duo dalam mendeteksi dengue akut menunjukkan bahwa SD Duo NS1 memberikan deteksi positif 100% antigen NS1 pada semua sampel dengue akut primer, sementara hanya 10% sampel dengue akut sekunder yang terdeteksi antigen NS1. Di sisi lain, 90% dari masing-masing sampel dengue akut primer dan sekunder teruji IgM positif oleh SD Duo IgM. Kombinasi SD Duo NS1/IgM memberikan tingkat deteksi positif masing-masing sebesar 100% dan 90% untuk infeksi dengue akut primer dan sekunder ( Tabel 3 ).
Tabel 3.
Kinerja kit SD BIOLINE Dengue Duo pada infeksi dengue primer dan sekunder
| Kategori | Angka (n) | Sampel yang diuji positif, n (%) | |||||
|---|---|---|---|---|---|---|---|
| RT-PCR | MAC-ELISA | SD DUO NS1 | SD DUO IgM | SD DUO IgG | SD DUO NS1/IgM | ||
| Dengue primer akut | 10 | 6 (60) | 10 (100) | 10 (100) | 9 (90) | 0 (0) | 10 (100) |
| Demam berdarah akut sekunder | 10 | 3 (30) | 10 (100) | 1 (10) | 9 (90) | 10 (100) | 9 (90) |
| Dengue primer konvalesen | 10 | 0 (0) | 10 (100) | 7 (70) | 10 (100) | 4 (40) | 10 (100) |
| Dengue sekunder yang sembuh | 10 | 0 (0) | 10 (100) | 0 (0) | 0 (0) | 10 (100) | 9 (90) |
Analisis data lebih lanjut menunjukkan bahwa tingkat deteksi NS1 berbanding terbalik, sedangkan tingkat deteksi IgM berbanding lurus dengan keberadaan antibodi IgG sebagaimana digambarkan oleh nilai HI ( Gambar 1 ). Pada kadar antibodi yang lebih rendah (HI ≤ 320), SD Duo NS1 memberikan tingkat deteksi yang lebih baik dibandingkan dengan kadar antibodi yang tinggi, sedangkan kadar antibodi yang tinggi (≥ 640 HI ≤ 10240) memberikan tingkat deteksi yang lebih baik untuk SD Duo IgM/IgG. Untuk diagnosis dengue akut, analisis gabungan SD Duo NS1 dan IgM/IgG memungkinkan diagnosis dini infeksi dengue akut yang lebih sensitif.
Gambar 1.
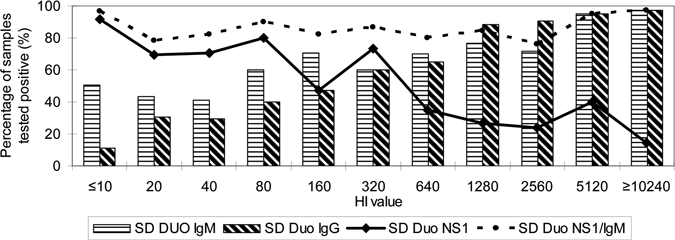
Data terkait hari timbulnya gejala penyakit yang sesuai dengan kit SD Dengue Duo ditentukan lebih lanjut. Seperti terlihat pada Gambar 2 , antigen NS1 dengue dapat dideteksi hingga Hari ke-12 sejak timbulnya demam, sedangkan RT-PCR hanya mampu mendeteksi RNA virus hingga Hari ke-8 pascainfeksi. Kit cepat SD Dengue Duo juga digunakan untuk mendeteksi sampel positif dengue yang terdiri dari keempat serotipe virus dengue ( N = 162) dan hasilnya disajikan pada Tabel 4. Tidak ada perbedaan signifikan dalam deteksi yang diamati antara keempat serotipe dengue ( P > 0,05).
Gambar 2.
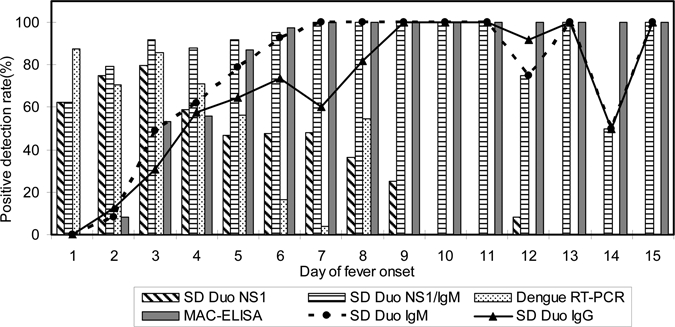
Tabel 4.
Perbandingan kinerja SD BIOLINE Dengue Duo dalam mendeteksi serotipe virus dengue *
| Diagnostik demam berdarah | Sensitivitas %, [95% CI] | Nilai P (antar kelompok) | |||
|---|---|---|---|---|---|
| DENV-1 ( N = 101) | DENV-2 ( N = 21) | DENV-3 ( N = 23) | DENV-4 ( N = 17) | ||
| SD Dengue Duo NS1 | 62,38 (63/101) [52,77–71,99] | 61,90 (13/21) [39,25–84,55] | 86,96 (20/23) [72,07–100] | 70,59 (12/17) [46,44–94,71] | 0.14 |
| SD Dengue Duo IgM | 57,43 (58/101) [47,62–67,24] | 57,14 (12/21) [34,06–80,22] | 43,48 (10/23) [21,56–65,40] | 41.18 (7/17) [15.10–67.26] | 0.44 |
| SD Dengue Duo NS1/IgM | 90,10 (91/101) [84,18–96,03] | 76,19 (16/21) [56,32–90,06] | 95,65 (22/23) [86,63–100] | 82,35 (14/17) [62,15–100] | 0.17 |
Uji χ 2 digunakan untuk analisis statistik (StatSoft, Inc.). Nilai P > 0,05 menunjukkan bahwa hasil tidak berhubungan secara signifikan.
Sensitivitas dan spesifisitas total kit cepat SD Dengue Duo dihitung berdasarkan sampel yang dianggap benar-benar dengue ( N = 185) melalui isolasi virus, RT-PCR, atau titer yang meningkat pada sampel berpasangan ( Tabel 5 ). Sensitivitas dan spesifisitas keseluruhan SD Duo NS1 adalah 65,41% (interval kepercayaan [IK] 95%: 58,49–72,32) dan 98,75% (IK 95%: 96,26–100) dengan efisiensi 75,47%, sedangkan SD Duo IgM memberikan sensitivitas 53,51% (IK 95%: 46,26–60,76) dan spesifisitas 100% dengan efisiensi 67,55%. Dengan menggabungkan kedua tes untuk NS1 dan IgM, SD Dengue Duo NS1/IgM memberikan kinerja yang lebih baik untuk mendeteksi demam berdarah akut, dengan sensitivitas keseluruhan sebesar 88,65% (95% CI: 84,04–93,26) dan spesifisitas sebesar 98,75% (95% CI: 96,26–100), dan efisiensi pengujian sebesar 91,70%.
Tabel 5.
Kinerja kit SD BIOLINE Dengue Duo dalam diagnosis demam berdarah
| Diagnostik demam berdarah | Sensitivitas, % ( N = 185) (95% CI) * | Spesifisitas, % ( N = 80) (95% CI) † | Efisiensi, % ( N = 265) (95% CI) | Nilai prediksi positif, % (95% CI) | Nilai prediksi negatif, % (95% CI) |
|---|---|---|---|---|---|
| SD Dengue Duo NS1 | 65,41 (121/185) [58,49–72,32] | 98,75 (79/80) [96,26–100] | 75,47 (200/265) [70,26–80,68] | 99,18 (121/122) [97,56–100] | 55,24 (79/143) [46,99–63,49] |
| SD Dengue Duo IgM | 53,51 (99/185) [46,26–60,76] | 100 (80/80) | 67,55 (179/265) [61,88–73,22] | 100 (99/99) | 48 (80/166) [40,32–55,68] |
| SD Dengue Duo NS1/IgM | 88,65 (164/185) [84,04–93,26] | 98,75 (79/80) [96,26–100] | 91,70 (243/265) [88,36–95,04] | 99,39(164/165) [91,68–100] | 79,0 (79/100) [71,29–86,71] |
Sampel positif sejati yang digunakan dalam analisis berasal dari kategori sampel berikut: isolasi virus positif ( N = 30), RT-PCR dengue ( N = 50), serum positif antigen NS1 dengue, yang juga positif untuk RT-PCR dengue ( N = 35), dan serum akut sero-negatif tetapi sero-konversi konvalesen ( N = 50), sampel primer akut ( N = 10), dan sampel sekunder akut ( N = 10).
Sampel negatif sejati berasal dari serum non-dengue, yang terdiri dari pasien dengan agen infeksius lain dan donor sehat.
Diskusi
Diagnosis laboratorium dini infeksi virus dengue akut penting untuk memberikan pengobatan yang tepat bagi pasien dan mencegah potensi wabah dengue. Saat ini, teknik yang paling umum digunakan di laboratorium untuk mendiagnosis infeksi virus dengue adalah isolasi virus, deteksi asam nukleat virus dengan RT-PCR, dan deteksi IgM spesifik dengue dengan MAC-ELISA. Meskipun isolasi virus dianggap sebagai standar emas untuk diagnosis laboratorium dengue, hal itu melelahkan dan memerlukan setidaknya 6–10 hari bagi virus untuk bereplikasi. 11 Di sisi lain, RT-PCR dan MAC-ELISA mahal, dan biasanya membutuhkan setidaknya setengah hari untuk menjalankan pengujian. Selain itu, fasilitas ini tidak tersedia secara luas di klinik dan rumah sakit. Oleh karena itu, kit tes cepat akan berguna untuk memberikan diagnosis dini infeksi dengue akut.
Keunggulan kit tes cepat SD Dengue Duo ini adalah dirancang untuk mendeteksi antigen NS1 virus dengue dan antibodi diferensial IgM/IgG terhadap virus dengue dalam darah manusia. Antigen NS1 umumnya ditemukan pada hari ke-1 hingga hari ke-9 setelah timbulnya demam. Deteksi anti-NS1 terhambat jika antibodi anti-NS1 diproduksi. Sementara itu, IgM dapat dideteksi pada hari ke-3 hingga ke-5 setelah timbulnya penyakit pada dengue primer dan pada hari ke-1 hingga ke-2 setelah timbulnya penyakit pada infeksi sekunder. 11 – 13 Keunikan perangkat kombinasi ini memungkinkan diagnosis dengue sedini hari pertama infeksi dengue.
Dalam studi ini, kami mengevaluasi penggunaan kit uji cepat SD Dengue Duo untuk diagnosis infeksi dengue. Strategi diagnostik yang menggabungkan SD Duo NS1 dan IgM digunakan dalam interpretasi hasil, karena ini dapat meningkatkan sensitivitas klinis keseluruhan dari kedua pengujian. Sensitivitas SD Duo NS1/IgM (88,65%) sebanding dengan studi terbaru. 4 , 5 , 21 – 23 Spesifisitas (98,75%) yang diamati dalam studi kami juga berkorelasi dengan semua studi sebelumnya. 4 , 5 , 21 – 23 Namun, sebagian besar menggunakan uji berbasis ELISA kecuali Vajpayee dkk. 21 dan Dussart dkk. 22 Namun, dalam studi mereka, ukuran sampel lebih kecil tetapi sebagian besar kesimpulan yang dibuat serupa. Analisis semua sampel dalam kelompok mengungkapkan bahwa deteksi dengue sejati paling rendah pada kelompok RT-PCR (88%), dan kelompok isolasi virus (70%). Sensitivitas tertinggi ditemukan pada kelompok dengue akut primer (100%), sedangkan pada kelompok serum dengue akut sekunder, sensitivitasnya lebih rendah, yaitu 90%. Sensitivitas tingkat deteksi yang jauh lebih rendah tercatat pada kelompok primer ketika SD Duo NS1 (85%) dan SD Duo IgM (95%) digunakan secara terpisah untuk mendeteksi dengue. Hal ini menunjukkan bahwa baik NS1 maupun IgM merupakan komponen penting dalam diagnosis dini dengue. Hal ini diperkuat oleh pengamatan bahwa keberadaan antibodi yang tinggi memberikan tingkat deteksi yang lebih baik untuk perangkat SD Duo IgM/IgG, sedangkan SD Dengue NS1 memberikan tingkat deteksi yang lebih baik pada kadar antibodi yang rendah seperti yang ditunjukkan pada Gambar 2 .
Spesifisitas untuk uji SD Dengue Duo terbukti 98% dengan hanya satu sampel yang terdeteksi antigen NS1. Namun, jenis sampel yang digunakan untuk menentukan spesifisitas terbatas dan lebih banyak sampel, terutama dari infeksi flavivirus lain seperti virus West Nile, virus St. Louis Encephalitis, virus Roccio, dan virus terkait dalam kelompok ini, perlu disertakan untuk memastikan cakupan yang memadai terhadap kemungkinan reaksi silang. Memperoleh serum yang negatif antibodi dengue terkadang tidak memungkinkan karena endemisitas yang tinggi di wilayah tropis dan juga dampak globalisasi. Alasan lainnya adalah semakin banyak individu yang terpapar beberapa flavivirus saat mereka bepergian ke berbagai daerah sebagai wisatawan.
Evaluasi ini menunjukkan bahwa kit tes cepat SD Dengue Duo bermanfaat untuk diagnosis dini infeksi dengue yang cepat. Evaluasi terbaru SD Dengue Duo NS1/IgM menunjukkan bahwa uji ini memiliki sensitivitas 88,65% (IK 95%: 84,04–93,26), spesifisitas 98,75% (IK 95%: 96,26–100), dan efisiensi uji 91,70%. Dengan mendeteksi NS1 dan IgM pada infeksi dengue, kit tes cepat SD Dengue Duo terbukti bermanfaat, sensitif, dan spesifik untuk diagnosis infeksi dengue akut.
Materi Tambahan
Ucapan Terima Kasih
Kami berterima kasih kepada SD Diagnostics, Inc., Korea, atas kemurahan hati menyediakan kit SD Dengue Duo, kepada para dokter dan perawat di University Malaya Medical Centre (UMMC), Kuala Lumpur, Malaysia, yang membantu dalam pengumpulan sampel; dan kepada para pasien atas partisipasi mereka dalam penelitian ini. Semua antibodi monoklonal yang digunakan dalam imunofluoresensi disediakan oleh Centre for Disease Control and Prevention, Fort Collins, Colorado. Kami berterima kasih kepada Kimberly Holloway dari National Microbiology Laboratory, Public Health Agency of Canada, dan Canadian Science Centre for Human and Animal Health, yang telah menyediakan sampel serum West Nile. Kami juga berterima kasih kepada Sutee Yoksan dari Center for Vaccine Development, Institute of Molecular Biosciences, Mahidol University di Salaya, yang telah menyediakan sampel serum ensefalitis Jepang.
Catatan: Data tambahan muncul di www.ajtmh.org .
Catatan kaki
Alamat penulis: Seok Mui Wang dan Shamala Devi Sekaran, Departemen Mikrobiologi Medis, Fakultas Kedokteran, Universitas Malaya, Kuala Lumpur, Malaysia, Email: seokmuiwang@yahoo.com dan shamalaya@yahoo.com .
Permintaan cetak ulang: Shamala Devi Sekaran, Departemen Mikrobiologi Medis, Fakultas Kedokteran, Universitas Malaya, Kuala Lumpur, 50603, Malaysia, Telp: 603-79675755, Faks: 603-79676672, E-mail: shamalaya@yahoo.com .
Referensi
- 1.Gubler DJ, Meltzer M. Dampak dengue/demam berdarah dengue pada negara berkembang. Adv Virus Res. 1999;53:35–70. doi: 10.1016/s0065-3527(08)60342-5. [ DOI ] [ PubMed ] [ Google Scholar ]
- 2.Organisasi Kesehatan Dunia. Buku Pegangan Organisasi Kesehatan Dunia. Jenewa: WHO; 2000. hlm. 1–84. (Demam berdarah dengue: diagnosis, pengobatan, dan pengendalian). [ Google Cendekia ]
- 3.Innis BL. Dalam: Infeksi Virus Eksotik. Porterfield JS, editor. London: Chapman & Hall Medical; 1995. hlm. 103–140. (Dengue dan demam berdarah dengue). [ Google Scholar ]
- 4.Blacksell SD, Mammen MP, Thongpaseuth S, Gibbons RV, Jarman RG, Jenjaroen K, Nisalak A, Phetsouvanh R, Newton PN, Day NP. Evaluasi deteksi antigen nonstruktural 1 virus dengue Panbio dan uji imunosorben terkait enzim antibodi imunoglobulin M untuk diagnosis infeksi dengue akut di Laos. Diagn Microbiol Infect Dis. 2008;60:43–49. doi: 10.1016/j.diagmicrobio.2007.07.011. [ DOI ] [ PubMed ] [ Google Scholar ]
- 5.Dussart P, Labeau B, Lagathu G, Louis P, Nunes MR, Rodrigues SG, Storck-Hermann C, Cesaire R, Morvan J, Flamand M, Baril L. Evaluasi enzim immunoassay untuk mendeteksi antigen NS1 virus dengue dalam serum manusia. Clin Vaccine Immunol. 2006;13:1185–1189. doi: 10.1128/CVI.00229-06. [ DOI ] [ Artikel gratis PMC ] [ PubMed ] [ Google Scholar ]
- 6.Kumarasamy V, Wahab AH, Chua SK, Hassan Z, Chem YK, Mohamad M, Chua KB. Evaluasi ELISA penangkapan antigen NS1 dengue komersial untuk diagnosis laboratorium infeksi virus dengue akut. J Virol Methods. 2007;140:75–79. doi: 10.1016/j.jviromet.2006.11.001. [ DOI ] [ PubMed ] [ Google Scholar ]
- 7.McBride W. Evaluasi kit uji dengue NS1 untuk diagnosis demam dengue. Diagn Microbiol Infect Dis. 2009;64:31–36. doi: 10.1016/j.diagmicrobio.2009.01.002. [ DOI ] [ PubMed ] [ Google Scholar ]
- 8.Sekaran SD, Lan EC, Mahesawarappa KB, Appanna R, Subramaniam G. Evaluasi uji ELISA penangkapan NS1 dengue untuk deteksi cepat dengue. J Infect Dev Ctries. 2007;1:182–188. [ Google Scholar ]
- Nomor 9Young PR, Hilditch PA, Bletchly C. Uji imunosorben terkait enzim penangkap antigen menunjukkan kadar protein NS1 virus dengue yang tinggi dalam serum pasien yang terinfeksi. J Clin Microbiol. 2000;38:1053–1057. doi: 10.1128/jcm.38.3.1053-1057.2000. [ DOI ] [ Artikel gratis PMC ] [ PubMed ] [ Google Scholar ]
- 10.Alcon S, Talarmin A, Debruyne M, Falconar A, Deubel V, Flammand M. Uji imunosorben terkait enzim spesifik untuk protein nonstruktural NS1 virus dengue tipe 1 menunjukkan sirkulasi antigen dalam darah selama fase akut penyakit pada pasien yang mengalami infeksi primer atau sekunder. J Clin Microbiol. 2002;40:376–381. doi: 10.1128/JCM.40.2.376-381.2002. [ DOI ] [ Artikel gratis PMC ] [ PubMed ] [ Google Scholar ]
- 11.Shu P, Huang J. Kemajuan terkini dalam diagnosis dengue. Clin Diagn Lab Immunol. 2004;11:642–650. doi: 10.1128/CDLI.11.4.642-650.2004. [ DOI ] [ Artikel gratis PMC ] [ PubMed ] [ Google Scholar ]
- 12.Gubler DJ. Diagnosis serologis demam berdarah dengue. Dengue Bull. 1996;20:20–23. [ Google Scholar ]
- 13.Innis B. Dalam: Dengue dan Demam Berdarah Dengue. Gubler DJ, Kuno G, editor. New York: CAB International; 1997. hlm. 221–243. (Respons antibodi terhadap infeksi virus dengue). [ Google Scholar ]
- 14.Deklarasi Helsinki dari Asosiasi Medis Dunia Prinsip-prinsip etika untuk penelitian medis yang melibatkan subjek manusia. JAMA. 2000;284:3043–3045. [ PubMed ] [ Google Scholar ]
- 15.Kuberski TT, Rosen L. Teknik sederhana untuk mendeteksi antigen dengue pada nyamuk dengan imunofluoresensi. Am J Trop Med Hyg. 1977;26:533–537. doi: 10.4269/ajtmh.1977.26.533. [ DOI ] [ PubMed ] [ Google Scholar ]
- 16.Gubler DJ, Kuno G, Sather GE, Velez M, Oliver A. Penggunaan kultur sel nyamuk dan antibodi monoklonal spesifik untuk surveilans rutin virus dengue. Am J Trop Med Hyg. 1984;33:158–165. doi: 10.4269/ajtmh.1984.33.158. [ DOI ] [ PubMed ] [ Google Scholar ]
- 17 tahunClarke DH, Cassals J. Teknik hemaglutinasi dan penghambatan hemaglutinasi dengan virus yang ditularkan melalui artropoda. Am J Trop Med Hyg. 1958;7:561–573. doi: 10.4269/ajtmh.1958.7.561. [ DOI ] [ PubMed ] [ Google Scholar ]
- 18 tahun.Organisasi Kesehatan Dunia. Pedoman Regional Pencegahan & Pengendalian Demam Berdarah Dengue/DBD. WHO/SEARO; 1997. (Penanganan epidemi demam berdarah dengue). [ Google Scholar ]
- 19 tahunLam SK, Devi S, Pang T. Deteksi IgM spesifik pada infeksi dengue. Southeast Asian J Trop Med Public Health. 1987;18:532–538. [ PubMed ] [ Google Scholar ]
- tanggal 20Yong YK, Thayan R, Chong HT, Tan CT, Sekaran SD. Deteksi cepat dan serotipe virus dengue dengan RT-PCR multipleks dan RT-PCR hijau SYBR waktu nyata. Singapore Med J. 2007;448:662–668. [ PubMed ] [ Google Scholar ]
- tanggal 21Vajpayee M, Singh UB, Seth P, Broor S. Evaluasi komparatif berbagai uji komersial untuk diagnosis demam berdarah. Southeast Asian J Trop Med Health. 2001;32:472–475. [ PubMed ] [ Google Scholar ]
- 22.Dussart P, Petit L, Labeau B, Bremand L, Leduc A, Moua D, Matheus S, Baril L. Evaluasi dua uji komersial baru untuk diagnosis infeksi virus dengue akut menggunakan deteksi antigen NS1 pada manusia. PLoS Negl Trop Dis. 2008;2:e280. doi: 10.1371/journal.pntd.0000280. [ DOI ] [ Artikel gratis PMC ] [ PubMed ] [ Google Scholar ]
- 23.Lapphra K, Sangsharaswichai A, Chokephaibulkit K, Tiengrim S, Piriyakarnsakul W, Chakorn T, Yoksan S, Wattanamongkolsil L, Thamlikitkul V. Evaluasi deteksi antigen NS1 untuk diagnosis infeksi dengue akut pada pasien dengan penyakit demam akut. Diagn Microbiol Infect Dis. 2008;60:387–391. doi: 10.1016/j.diagmicrobio.2007.11.010. [ DOI ] [ PubMed ] [ Google Scholar ]
Kami adalah penyedia alat kesehatan dan laboratorium,info lanjut 087849378899